1.AKCIJA
U ambulantu dolazi pacijent u dobi od 67 godina na konzultaciju nakon kontrolnog pregleda gastroenterologa.
Obiteljska anamneza: otac boluje od hipertenzije, majka umrla od CVI s 80 godina
Osobna anamneza: M17 Gonartroza /artroza koljena, M50 Bolesti cervikalnog diska, K29 Gastritis i duodenitis, K51 Ulcerozni kolitis, M72.0 Palmarna fascijalna fibromatoza /Dupuytren, M75 Oštećenja ramena, H90.3 Perceptivni gubitak sluha, obostrani, I10 Arterijska hipertenzija
Funkcije i navike: apetit dobar. Stolica uredna, redovita, bez patoloških primjesa. Mokrenje uredno. Uzima pola litre vina dnevno, nepušač.
Lijekovi: Emanera (ezomeprazol) a 20 mg 1×1, Pentasa (mesalazin) a 500 mg 1×1, Co-Perineva ( perindopril/ indapamid) a 4 mg/ 1,25 mg) 1×1
Alergije na lijekove: nema
Sadašnja bolest: U ambulantu dolazi pacijent u dobi od 67 godina na konzultaciju, donosi nalaz kontrole gastroenterologa.
Inače se unazad 10 godina kontrolira po gastroenterologu radi kroničnog gastritisa (u 2 navrata HP pozitivan- provedena eradikacijska terapija). U navedenom periodu se prate povišene razine feritina (682-1071) i GGT (74-102). Unazad godinu dana navodi pojačan umor i pospanost. Bio privatno kod gastroenterologa kada je UZV abdomena nađena jetra nešto grublje ehostrukture parenhina, ostalo uredno. Sada bio na redovnoj kontroli gastroenterologa kada je postavljena sumnja na hemokromatozu (feritin 1130). Preporučeno učiniti gensko testiranje, indicirana flebotomija 1x tjedno / 3 tjedna. Potom kontrola KKS, Fe, feritin, kontrola gastroenterologa s nalazima.
Iz statusa: pri svijesti, u kontaktu, orijentiran u sva tri pravca. Koža i vidljive sluznice uredno hidrirane i prokrvljene, bez osipa. Srce: akcija ritmična, tonovi jasni, šum ne čujem. Pulmo: obostrano uredan šum disanja. Abdomen: mekan, bezbolan, čujne peristaltike, bez organomegalije. Ekstremiteti urednih perifernih arterijskih pulzacija, bez edema.
Iz nalaza: UZV abdomena: jetra uredne veličine, pravilnih kontura, nešto grublje i reflektivnije ehostrukture, bez vidljivih fokalnih lezija. Ostalo uredno. KKS bo, Fe 30, UIBC 23, feritin 1130. Nalaz dosta uvjerljivo govori za hemokromatozu. Gensko testiranje se može napraviti u nekoj od Klinika. Neovisno o tome potrebno je započeti terapiju venepunkcijama (450 ml 1x tjedno na Odjelu za transfuziologiju). Napraviti ukupno 3 postupka, potom kontrola KKS i feritina 4 tjedna od zadnjeg postupka.
Dg: K76 Ostale bolesti jetre, Hemokromatoza
Th: ad Transfuzijska medicina, venepunkcije, restrikcija alkohola
Pacijentu se objasni kako se radi o bolesti u kojoj se pojačano nakuplja željezo u tijelu koje prvenstveno može dovesti do oštećenja jetre i zglobova, stoga je višak potrebno izbaciti iz tijela a to činimo redovitim uzimanjem krvi. Također je vrlo važno da u potpunosti izbaci unos alkohola.
Konzultacija: ostavio kontrolni nalaz gastroenterologa: feritin 572, uredna krvna slika, kontrola feritina za 2 mjeseca pa dogovor za dalje.
Kontrolni pregled: traži uputnicu za kontrolni laboratorij i kontrolni pregled gastroenterologa. Također navodi kako unazad mjesec dana ima pritisak u glavi, nema ravnoteže, ima osjećaj da mu se slike miču., pojačano zaboravlja.
Fizikalni pregled: RR 132/76 mmHg, c/p 66/min, RF 13/min, SaO2 98%. KP kompenziran. Srce: akcija ritmična, tonovi jasni, šum ne čujem. Pulmo: uredan šum disanja. Neurološki: nistagmusa nema, HINTS bez patologije, u Rombergu titubira, Tandem hod izvodi nestabilno, pokus prst-nos-prst i peta-koljeno izvodi, napeta oba trapezijusa, pokreti u cervikalnoj kralježnici ograničeni u svim smjerovima, navodi nelagodu.
Ad lab: KKS, glukoza, HbA1c, AST, ALT, GGT, kolesterol, LDL, HDL, trigliceridi, kreatinin, kompletna pretraga urina, feritin. Ad Kontrolni pregled gastroenterologa.
Th: Nalgesin forte a 550 mg 2×1 + Normabel a 5 mg 1×1 + IPP, lokalno masaža, NSAID gel+ vježbe za vratnu kralježnicu. Kontrola 5-7 dana ako ne prođe, po potrebi ranije. Dan MoCA test.
Konzultacija: zove radi uvida u laboratorijski nalaz: feritin 213, GGT 72, kolesterol 6.4, LDL 4.4. trigliceridi 1.3, HDL 1.4, ostalo uredno. Na upit je li obavio genetsko testiranje na hemokromatozu navodi da nije te ga se pokuša ponovo motivirati da isto učini. Kontrola s kontrolnim nalazom gastroenterologa.
2.OSVRT NA UČINJENO
U ovom slučaju prikazan je pacijent kod kojeg su se tokom niza godina pratile povišene razine serumskog feritina i GGT, a potom su se javili i simptomi u vidu umora i poremećaja spavanja. Na kontrolnom pregledu gastroenterologa UZV abdomena je pokazao strukturalne promjene jetre, dok je biokemijska analiza krvi pokazala vrijednosti feritina >1000 μg/L. na temelju navedenoga postavljena je dijagnoza hemosideroze te se pristupilo terapijskim venepunkcijama na što dolazi do pada vrijednosti feritina i povlačenja tegoba. Pacijentu je također savjetovano učiniti genetsku analizu, međutim nije iskazao zainteresiranost jer mu je naporno putovati u drugi grad.
3.EDUKATIVNA KORIST IZ PRIMJERA
Nasljedna hemokromatoza je autosomno recesivni poremećaj u kojem je poremećena regulacija željeza, što rezultira toksičnim nakupljanjem željeza u vitalnim organima i razvojem ciroze, bolesti kostiju i zglobova, dijabetes melitusa i bolesti srca. To je najčešća genetska bolest u bijelaca. Muškarci imaju 24 puta veću stopu bolesti preopterećenja željezom u usporedbi sa ženama. Osobe koje su homozigoti za HFE gensku mutacija C282Y čine 85 – 90 % sveukupno oboljelih osoba. Oštećenje krajnjih organa ili kliničke manifestacije nasljedne hemokromatoze javljaju se u otprilike 10 % osoba homozigotnih za C282Y.
Ono što je postalo jasno tokom proteklih 20 godina je heterogenost kliničke ekspresije same bolesti, uključujući spolne razlike, kao i nespecifičnost serumskih razina željeza i serumske saturacije transferina (TSAT=Fe / TIBC x 100), što je dovelo do promjene dijagnostičkih kriterija.
METABOLIZAM ŽELJEZA
Željezo je raspoređeno u metabolički aktivna područja i u zalihe. Ukupna količina željeza u tijelu je oko 3,5 g kod zdravih muškaraca i 2,5 g kod žena; razlika se odnosi na manju veličinu ženskog tijela, i manju količinu pohranjenog željeza zbog gubitka tijekom menstruacije. Raspodjela željeza u tijelu je:
- Hemoglobin: 2 g (muškarci), 1,5 g (žene)
- Feritin: 1 g (muškarci), 0,6 g (žene)
- Hemosiderin: 300 mg
- Mioglobin: 200 mg
- Tkivni enzimi (hem i nehem): 150 mg
- Željezo u transportu: 3 mg
Apsorpcija željeza
Apsorpcija željeza odvija se u duodenumu i gornjem jejunumu. Apsorpcija željeza ovisi o molekularnom obliku željeza i drugim tvarima unesenim hranom. Željezo se najbolje apsorbira iz hrane koja sadrži željezo u obliku hema (meso). Željezo koje nije u obliku hema, a koje je prisutno u dijetalnoj hrani, je obično u feri obliku, te se treba reducirati u fero oblik i osloboditi od vežućih tvari iz hrane pomoću želučanog soka. Apsorpcija željeza, koje nije u obliku hema, je smanjena zbog drugih sastojaka hrane (npr. fitati i polifenoli iz biljnih vlakana, tanati i fosfoproteini iz čaja, mekinje) i nekih antibiotika (npr. tetraciklin). Askorbinska kiselina je jedini uobičajeni sastojak hrane koji povećava apsorpciju takvoga željeza.
Prosječna prehrana, koja sadrži oko 6 mg elementarnog željeza/1000 kcal hrane, je dovoljna za homeostazu željeza. Od oko 15 mg dnevnog unosa željeza hranom, odrasle osobe apsorbiraju tek oko 1 mg, što je i približna količina dnevnog gubitka, deskvamacijom stanica kože i crijeva. Kod nedostatka željeza, apsorpcija se povećava zbog supresije hepcidina, ključnog regulatora metabolizma željeza; međutim, apsorpcija se rijetko povećava na > 6 mg/dan, osim ako se primjenjuju nadomjesci željeza. Djeca imaju veće potrebe za željezom i smatra se da apsorbiraju više željeza kako bi se zadovoljila ova potreba.
Prijenos i iskorištavanje željeza
Željezo se iz stanica crijevne sluznice prenosi na transferin, protein koji se stvara u jetri i prenosi željezo u krvi; transferin može prenijeti željezo iz stanica (crijeva, makrofaga) do specifičnih receptora na eritroblastima, te stanicama posteljice i jetre. Prilikom sinteze hema, transferin doprema željezo do mitohondrija eritroblasta, koji ga ugrađuju u protoporfirin, čime nastaje hem. Transferin (plazmatski poluvijek života 8 dana) se nakon toga istiskuje iz stanice te ponovno iskorištava. Stvaranje transferina je povećano kod nedostaka željeza, ali je smanjeno kod svih vrsta kroničnih bolesti.
Skladištenje i recikliranje željeza
Željezo koje se ne koristi za eritropoezu, prenosi se transferinom do zaliha; željezo se skladišti u 2 oblika, kao feritin i hemosiderin. Najvažniji je feritin (heterogena skupina proteina koja okružuje željeznu jezgru), koji je topljiv, te služi za pohranu željeza u jetri (hepatociti), koštanoj srži, i slezeni (makrofagi). Željezo pohranjeno u obliku feritina je brzo dostupno za bilo kakvu potrebu u organizmu. Cirkulirajuća (serumska) razina feritina je mjerilo veličine zaliha željeza u tijelu (1 ng/ml = 8 mg željeza u skladištu). Drugi oblik skladištenja željeza je hemosiderin, koji je relativno netopljiv i nalazi se pretežno u jetri (u Kuppferovim stanicama) i u koštanoj srži (u makrofazima).
Budući da je apsorpcija željeza ograničena, organizam reciklira i čuva željezo. Transferin hvata i reciklira željezo iz ostarjelih eritrocita koje su fagocitirali mononukleari. Taj mehanizam osigurava oko 97% dnevnih potreba za željezom (oko 25 mg). Starenjem se zalihe željeza povećavaju zbog usporenog izlučivanja željeza.
GENETIKA
U bolesnika s nasljednom hemokromatozom, glavni defekt gena mijenja ekspresiju HFE proteina odgovornog za regulaciju hepcidina, primarnog hormona za regulaciju željeza. Kao odgovor na višak željeza, hepatociti luče hepcidin, koji smanjuje intestinalnu apsorpciju željeza od strane enterocita i smanjuje otpuštanje željeza od strane makrofaga. Time se održava razina željeza u fiziološkom rasponu. Kada gen HFE pokazuje missense mutaciju na poziciji aminokiseline 282, proteinski produkt (C282Y) uzrokuje smanjenu ekspresiju hepcidina kao odgovor na povišene razine željeza i naknadnu nereguliranu kontrolu razina željeza. Otprilike 85 do 90 % oboljelih pacijenata su homozigoti za mutaciju C282Y.
Nasljedna hemokromatoza češća je u populaciji bijele rase sjevernoeuropskog podrijetla i najčešća je u Irskoj ; prevalencija se kreće od jedne na 150 do 250 osoba. Međutim, budući da samo 10 % (jedan od 2500) onih s homozigotnošću C282Y ima oštećenje krajnjih organa ili kliničke manifestacije nasljedne hemokromatoze, većina osoba koje su pozitivne na nasljednu hemokromatozu su asimptomatske. Iako postoje druge HFE genske mutacije, rijetko su povezane s oštećenjem organa povezanim sa željezom.
BIOKEMIJSKE MANIFESTACIJE HEMOKROMATOZE
Hemokromatoza se može očitovati elevacijom serumske saturacije transferina (TSAT), razine feritina ili hematoloških nalaza. Kako su laboratorijski nalazi vezano za željezo varijabilni, potrebno je patološki nalaz dokumentirati u više uzastopnih mjerenja. Najranija manifestacija bolesti je povišenje serumske saturacije transferina (TSAT), razine hemoglobina (Hb) i volumena eritrocita (MCV). Te promjene prethode povišenju razine serumskog feritina. Najveće abnormalnosti zabilježene su u pojedinim homozigotima (C282Y) i to češće u muškaraca. Povišenje saturacije trasferina (≥45%) ima osjetljivost od 94% u muškaraca i 73% u žena za detekciju navedene mutacije. Razine serumskog feritina >300 μg/L u muškaraca ima osjetljivost od 88%, a u žena >200 μg/L ima osjetljivost od 57%. Saturacija transferina <45% u kombinaciji sa normalnim razinama serumskog feritina ima negativnu prediktivnu vrijednost od 97% kako za muškarce tako i za žene. Oko 8% homozigotnih žena sa mujtacijom C282Y i oko 44% homozigotnih muškaraca sa navedenom mutacijom ima serumske razine feritina >1000 μg/L, iznad koje morbiditet značajno raste. Limitiranost korištenja serumskih razina feritina u detekciji navedene mutacije je u tome što je serumski feritin povišen u do 40% osoba koje nemaju ni varijacije u mutacijama ni preopterećenje željezom, već su najvjerojatnije odraz pretilosti na razine serumskog feritina. U mutaciji C282Y homozigota postoji korelacija između serumskih razina feritina i tjelesnih zaliha željeza, bazirano na koncentraciji željeza u jetri, što izostaje kod osoba koje nemaju hemokromatozu. Prema tome, u odsutnosti navedene mutacije ili sekundarnog poremećaja preopterećenja željezom, povišene razine serumskog feritina nisu dokaz preopterećenja željezom.
Povišene vrijednosti volumena eritrocita (MCV) > 94 fl identificira 34% svih muškaraca i 62% svih žena sa hemokromatozom. Međutim, 4% opće populacije ima MCV >94 fl, od kojih njih 96% nema mutaciju. Najveća klinička prednost te metode detekcije je da omogućuje naknadni benefit probira na temelju ostalih laboratorijskih parametara.
SIMPTOMI
Osobe s nasljednom hemokromatozom obično su asimptomatske, osobito u ranim fazama. Kada su prisutni, simptomi su nejasni i nespecifični. Osim toga, pacijenti se rijetko javljaju s klasičnim kliničkim trijasom “brončanog dijabetesa” ciroze, dijabetesa i brončane pigmentacije kože. Simptomatska nasljedna hemokromatoza rijetko se javlja u osoba mlađih od 40 godina. Kod žena menstruacija odgađa nakupljanje željeza; stoga simptomi obično počinju nakon menopauze, histerektomije ili produljene uporabe kontinuiranih oralnih kontraceptiva. Najčešći prisutni simptomi su slabost, letargija, impotencija i artralgije . Kasnije manifestacije uključuju artralgije, osteoporozu, cirozu, hepatocelularni karcinom, kardiomiopatiju, aritmiju, dijabetes melitus i hipogonadizam. Fizikalni nalazi mogu uključivati više organskih sustava. Mnoge značajke upućuju na druge bolesti osim nasljedne hemokromatoze. Sve bolesnike s abnormalnim rezultatima testova jetrene funkcije ili drugim pokazateljima jetrene bolesti treba procijeniti na nasljednu hemokromatozu.
Simptomi su nespecifični sa često jednakom prevalencijom u osoba sa i bez hemokromatoze. Najčešći simptom, umor, zabilježen je primarno kod muškaraca sa serumskim razinama feritina >1000 μg/L.
Bolest jetre
Uznapredovala jetrena fibroza i ciroza (Scheuer stadij F3 ili F4) rijetke su u mlađih od 45 godina bez drugih bolesti jetre. Pojavljuje se u od prilike 8% žena i 25% muškaraca sa hemokromatozom. Rizični faktori uključuju ekscesivnu konzumaciju alkohola, dijabetes, artritis, povišene razine serumskog feritina >1000 μg/L, trombocite <200 x10(9)/L, povišen AST, koncentracija željeza u jetri >200 μmol/g i željezo evakuirano flebotomijom >9,6 g. Muškarci homozigoti imaju životni rizik za nastanak primarnog karcinoma jetre 12x veći od muškaraca bez HFE varijacije (7.2% vs. 0.6%). Nema značajne povezanosti između homozigota i karcinoma jetre u žena. Pacijenti sa uznapredovalom jetrenom fibrozom u povećanom su riziku za primarni karcinom jetre (hepatocelularni ili kolangiokarcinom) te se trebaju redovito kontrolirati UZV-om svakih 6 mjeseci. Kontrola je dugoročna pošto rizik za nastanak karcinoma perzistira dokle perzistira ciroza. Regresija uznapredovale jetrene fibroze na Scheuer stadij F2 ili manji povezana je sa značajnom redukcijom od dugoročnog rizika za nastanak hepatocelularnog karcinoma, iako većina slučajeva ciroze perzistira i nakon liječenja. Kada se takva regresija postigne, kliničari mogu razmotriti rjeđe UZV kontrole. Razine serumskog željeza na gornjoj granici normalnog raspona ali u odsutnosti preopterećenja željezom, rizični su faktor za primarni karcinom jetre, podupirući direktnu ulogu željeza u karcinogenezi. Nadalje, terapeutska flebotomija značajno smanjuje rizik za rak, dodajući daljnji kredibilitet ulozi željeza u nastanku karcinoma.
Artritis
Pogađa barem 24% bolesnika i glavni je uzrok invalidnosti i smanjene kvalitete života. Klasično, artropatija zahvaća metokarpofalangealne zglobove, posebno prvi i treći. Slijede kuk, gležanj, radiokarpalni zglobovi, lakat, rame i koljeno, kao i lumbalna kralježnica. Često je teško razlikovati artritis uzrokovan hemokromatozom od degenerativnog osteoartritisa (poznat i kao tip 1 poliartikularni artritis) koji je karakteriziran Heberdenovim i Buchardovim čvorićima koji najčešće zahvaća interfalangealne zglobove, koljena i metatarzofalangealni zglob nožnog palca a pojavljuje se s jednakom učestalošću u pacijenata sa hemokromatozom kao i u onih bez nje. Međutim, tip 2 poliartikularnog artritisa, karakteriziran metatarzofalangealnom artropatijom 2-5 prsta ili bilateralnim zahvaćanjem velikih zglobova (radiokarpalni zglob, lakat, kuk, koljeno, gležanj) 8x je češći u osoba sa hemokromatozom nego u onih bez nje. Nejasno je zašto artropatija zahvaća samo manji dio osoba sa hemokromatozom. Artritis se može javiti u bilo koje vrijeme tokom razvoja bolesti, čak i nakon uspješne flebotomije. Rizični faktori za artritis uključuju stariju dob, uznapredovalu fibrozu jetre, serumske razine feritina >1000 μg/L i serumska saturacija transferina >50% barem tokom 6 godina. Bolesnici sa hemokromatozom i artritisom imaju značajno višu razinu srednjeg volumena eritrocita u odnosu na one bez artritisa ili koji imaju ostale varijante artritisa (reumatoidni, osteoartritis) ali u odsutnosti HFE varijante. Bolest jetre i artritis imaju težnju da se pojave istovremeno. Artritis je vjerojatniji kod viših razina željeza ili uznapredovanije bolesti jetre. Izostanak artritisa ima negativnu prediktivnu vrijednost od 95% za uznapredovalu fibrozu jetre.
Ostale kliničke manifestacija
Sa hemokromatozom povezana su brojna stanja kao što su hiperpigmentacija, dijabetes melitus, hipogonotropni hipogonadizam i kardiomiopatija. Osobe sa hemokromatozom su također pod povećanom opasnosti od infekcije Vibrio vulnificuns i oportunističkim infekcijama. Navedena stanja se najčešće zbrinjavaju u sklopu standardne njege i u nastavku uobičajenog liječenja preopterećenja željezom. Kardiomiopatije je rijetka komplikacija koja je potencijalno reverzibilna terapijom micanja željeza.
Nasljedna hemokromatoza povezana je sa zloćudnim bolestima, osobito hepatocelularnim karcinomom. Približno 6 % bolesnika s nasljednom hemokromatozom i cirozom razvije hepatocelularni karcinom; to predstavlja 20 puta veći životni rizik u odnosu na opću populaciju i godišnju stopu incidencije od 4 %. Mehanizam povećanog rizika je učinak viška željeza u poticanju oksidativnog oštećenja DNA i aktivnosti slobodnih radikala. Povećane zalihe željeza također mogu povećati rizik od raka dojke, iako je literatura ograničena i proturječna.
Preopterećenje željezom uzrokuje restriktivnu kardiomiopatiju, dijastoličku disfunkciju, zatajenje srca, aritmije i poremećaje provođenja, što može dovesti do atrioventrikularnog bloka, bradiaritmija, tahiaritmija i iznenadne srčane smrti. Kardiomiopatija preopterećenja željezom je reverzibilna ako terapija započne prije pojave očitog zatajenja srca.
Preživljavanje može biti skraćeno u onih s cirozom ili dijabetesom; rana dijagnoza i liječenje mogu spriječiti pobol i smrtnost. Petogodišnja stopa preživljenja kod pacijenata koji imaju neliječenu nasljednu hemokromatozu i cirozu je smanjena za 50 % u usporedbi s onima koji nemaju cirozu. Nadalje, bolesnici s nasljednom hemokromatozom koji konzumiraju više od 60 g alkohola dnevno (oko četiri porcije) imaju deveterostruko povećanje incidencije ciroze.
DIJAGNOZA
Za dijagnozu je potrebna potvrda povišene razine feritina u serumu i zasićenja transferina, sa ili bez simptoma. Subtipizacija se temelji na genotipskoj ekspresiji. Mjerenje serumskog feritina najkorisniji je prognostički pokazatelj težine bolesti.
Postoje 3 scenarija za koje postoji algoritam kliničke procjene hemokromatoze: pozitivna obiteljska anamneza bez prisutstva simptoma; povišene vrijednosti serumskog transferina, feritina ili aminotransferaza u odsustvu simptoma; ili prisustvo simptoma.
Asimptomatske osobe sa pozitivnom obiteljskom anamnezom
Kod djece homozigota sa poznatom mutacijom C282Y mlađom od 18 godina, prihvatljiv pristup je odrediti genotip oba roditelja, pošto je pojava bolesti prije 18. godine izuzetno rijetka. Ukoliko jedan od roditelja nema navedenu mutaciju, nema rizika da potomstvo bude homozigot. Za osobe ≥18. godina ili kod kojih nije moguće provesti genotipizaciju roditelja, genetsko testiranje treba provesti što prije kako bi se odredio genotip i s njim povezan rizik za preopterećenje željezom. Serumske razine saturacije transferina i feritina trebale bi se mjeriti samo u visoko rizičnih i nisko rizičnih pacijenata- ukoliko su razine povišene daljnji postupak treba provesti kako je opisano dalje u tekstu za kliničku procjenu simptomatskih osoba. Ukoliko serumske razine feritina nisu povišene, daljnja mjerenja treba ponoviti u narednih 5 godina kako bi detektirala progresija. U homozigota ≥55 godina koje imaju razine serumskog feritina u granicama normale, daljnje kontrole možemo obustaviti, pošto je malo vjerojatno da će se opterećenje željezom ikada razviti. U žena, razine serumskog feritina generalno dosežu plato 10-20 godina nakon menopauze, u razinama koje ne prelaze 400 μg/L, i koje su premale da bi se razvila bolest. Homozigotima treba savjetovati screening rođaka u prvom koljenu te ih pratiti radi mogućeg razvoja kolorektalnog karcinoma i karcinoma dojke.
Asimptomatske osobe sa povišenim laboratorijskim vrijednostima parametara željeza
Serumska saturacija transferina, razine feritina ili razina aminotransferaza u pravilu su povišeni u općoj populaciji. Povišene razine serumskog transferina i razine feritina nalazimo povišene u 6% -40% odraslih osoba. Do 14% odraslih ima povišene vrijednosti alanin aminotransferaze (ALT). Za osobe podrijetlom iz Sjeverne Europe koje imaju povišene vrijednosti serumskog feritina i saturacije transferina najispravnije daljnje postupanje je testiranje na mutaciju C282Y. U osoba sa abnormalnim razinama aminotransferaza treba učiniti mjerenje serumske koncentracije feritina i saturacije transferina. Ukoliko su razine povišene a osoba je podrijetlom iz Sjeverne Europe treba učiniti genetsko testiranje na p.C282Y. Potvrđeni homozigoti, ali i osobe koje nisu podrijetlom iz Sjeverne Europe ali imaju povišene vrijednosti serumske saturacije transferinom i feritina, trebaju se procijeniti kao što će biti objašnjeno u nastavku. Rijetko se nađe klinički značajno opterećenje željezom u osoba podrijetla iz Sjeverne Europe sa povišenim serumskim razinama feritina i saturacije transferina a da nisu homozigoti za C282Y.
Simptomatski pacijenti
Procjena treba biti u smislu da se utvrdi rizik oštećenja ciljnih organa, posebice jetre i zglobova (artritis). Rizik od artritisa i uznapredovale jetrene fibroze i posljedično razvoja primarnog karcinoma jetre raste sa progresijom odlaganja željeza, posebice kad serumske razine željeza porastu >1000 μg/L. Sa hemokromatozom povezani artritis veoma je koristan klinički prediktor prisutnosti uznapredovale jetrene fibroze. Za homozigote sa dodatnim rizičnim faktorima za bolest jetre moguće će biti potrebna procjena zahvaćanja jetre kod nižih razina feritina. Kvantifikacija koncentracije željeza u jetri i procjena stadija fibroze jetre ključna je u procjeni rizika nastanka uznapredovale fibroze jetre i primarnog karcinoma jetre i treba se rutinski provoditi u svih osoba sa serumskom razinom feritina >1000 μg/L ili artritisom ili su na drugi način pod povećanim rizikom zbog dodatnih faktora kao neobjašnjena hepatomegalija ili povišene razine serumskih aminotransferaza.
Analiza mutacije HFE smanjila je upotrebu biopsije jetre, koja je obično rezervirana za određivanje stupnja fibroze ili ciroze kod osoba homozigotnih za C282Y koje imaju razinu feritina u serumu od najmanje 1000 μg / ml. Osobe s cirozom mogući su kandidati za transplantaciju jetre nakon procjene gastroenterologa ili hematologa. U bolesnika s C282Y heterozigotnošću i izrazito povišenim razinama feritina, biopsija jetre ili neinvazivne specijalizirane tehnike magnetske rezonancije mogu se koristiti za određivanje stupnja sadržaja željeza u jetri ili za dijagnosticiranje neklasične hemokromatoze.
Kvantifikacija koncentracije željeza u jetri pomaže u procjeni rizika od nastanka fibroze. U prošlosti se koncentracija željeza utvrđivana na temelju biopsije jetre ali sada su dostupne neinvazivne metode kvantifikacije, npr. izračun na temelju dobivenog željeza nakon terapeutske flebotomije do postizanja razina serumskog feritina od 50-100 μg/L ili izračun na temelju magnetske rezonance. Magnetska rezonanca ima dobru kliničku vrijednost za određivanje koncentracije željeza u jetri i miokardu. Koncentracija željeza u jetri može se mjeriti biokemijski i nakon biopsije jetre. Na navedene načine može se detektirati uznapredovala jetrena fibroza čija je procjena ključna u određivanju prognoze i rizika za nastanak hepatocelularnog karcinoma. Sve osobe sa uznapredovalom fibrozom jetre u opasnosti su od razvoja primarnog karcinoma jetre te s tim u skladu trebaju pojačan nadzor i praćenje u svrhu pravodobne dijagnoze istoga.
Usporedni laboratorijski nalazi u osoba s poremećajima željeza
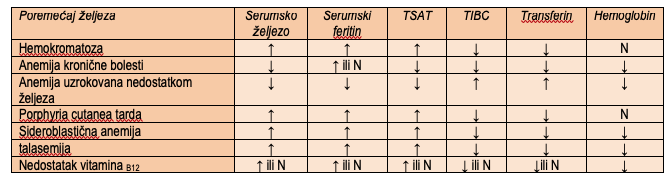
Stope ciroze u bolesnika s nasljednom hemokromatozom
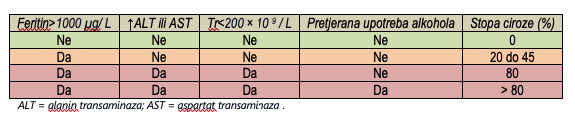
LIJEČENJE
Svi pacijenti s homozigotnom nasljednom hemokromatozom i dokazima o preopterećenju željezom (tj. TSAT> 45 % i razina feritina u serumu > 300 ng / ml kod muškaraca i > 200 ng po ml kod žena) treba liječiti, bez obzira na simptome. Iako nisu provedena randomizirana kontrolirana ispitivanja, standard liječenja je flebotomija kako bi se smanjile ukupne razine željeza u tijelu i postigle normalne razine feritina, a učestalost se određuje serijskim mjerenjima razine feritina u serumu i zasićenja transferina. Razine hemoglobina treba provjeriti prije svake flebotomije, a terapija se obično obustavlja kada je razina hemoglobina <125 g / L. Terapija je podijeljena na sam terapijski zahvat i faze održavanja. Terapija se sastoji od tjednih flebotomija dok se ne postigne serumska razina feritina od 50-100 μg/L. Potom slijede faze održavanja koje imaju za cilj održati postignutu razinu serumskog feritina. Bolesnici bi se tijekom liječenja trebali pridržavati smjernica za probir raka debelog crijeva u općoj populaciji, osobito ako dođe do nedostatka željeza.
Očekivane dobrobiti terapeutske flebotomije uključuju sljedeće: smanjenje zaliha željeza u tkivu na normalne razine; rješavanje umora i letargije; izrazito smanjenje bronzanosti/pigmentacije kože; značajno poboljšanje abnormalnosti jetrenih enzima, bol u desnom gornjem kvadrantu i hepatomegalija, ako je prisutna u početku; preokret fibroze jetre u 30 % slučajeva; poboljšana srčana funkcija; i povremeno poboljšanje kontrole dijabetesa. Međutim, liječenje flebotomijom neće poništiti utvrđenu cirozu ili značajno poboljšati artropatiju, atrofiju testisa ili disfunkciju štitnjače. Ukoliko ciroza perzistira nema jasnog dokaza da flebotomija smanjuje rizik od nastanka primarnog karcinoma jetre, ublažuje uznapredovali artritis ili je učinkovita u terapiji sekundarnog dijabetesa melitusa koji je posljedica hemokromatoze.
Izbjegavanje konzumiranja sirovih morskih plodova u svrhu smanjenja rizika od infekcije V. vulnificus te redukcija konzumacije alkohola radi smanjenja rizika nastanka uznapredovale fibroze jetre trebaju se provoditi istovremeno sa flebotomijom. Ako pacijenti ne podnose flebotomiju, terapija keliranjem željeza je opcija druge linije.
Avidnost željeza je komplikacija flebotomije. Definirano kao žarka želja ili žudnja za željezom, ovo stanje predstavlja prekomjernu korekciju preopterećenja željezom. Klinički, pacijenti će imati niske ili normalne razine feritina u serumu (oblik skladištenja željeza), ali će ipak imati povišenu zasićenost transferina (mobilizirani oblik željeza). Budući da je povišena zasićenost transferina početni pokazatelj nasljedne hemokromatoze, ove laboratorijske nalaze može biti teško uskladiti, što dovodi do podcjenjivanja avidnosti željeza. Ako se pojavi avidnost željeza, može biti povezana anemija koja zahtijeva procjenu gastrointestinalnog izvora krvarenja. Paradoksalno, liječenje avidnosti željeza u pacijenata s nasljednom hemokromatozom može uključivati nadoknadu željeza dok se zasićenje transferina i razine feritina u serumu ne vrate na normalu.
Promjene u prehrani općenito su nepotrebne. Ravnoteža željeza obično se čvrsto održava; apsorbirana dnevna prehrambena količina odgovara količini izgubljenoj svaki dan unutar očišćenih stanica ili približno 1 mg. S obzirom da bolesnici s nasljednom hemokromatozom mogu apsorbirati do 4 mg željeza dnevno, treba izbjegavati suplemente željeza, kao i suplementaciju vitamina C. Iako neki autori preporučuju specifične promjene u prehrani za smanjenje razine željeza u serumu, nikakvi podaci nisu pokazali da manipulacija prehranom poboljšava ishode pacijenata. Treba napomenuti da treba izbjegavati sirove školjke zbog Vibrio vulnificus , bakterije koja može uzrokovati potencijalno smrtonosnu infekciju i koja je zabilježena kod pacijenata s visokim razinama željeza. Povišene zalihe željeza mogu oslabiti učinkovito baktericidno djelovanje hepcidina.
PROBIR
Univerzalni probir na nasljednu hemokromatozu se ne preporuča, ali testiranje treba provesti u srodnika u prvom koljenu bolesnika s klasičnom hemokromatozom. ili za dijagnosticiranje neklasične nasljedne hemokromatoze u bolesnika s drugim genetskim defektima. Djeca čiji je jedan roditelj s nasljednom hemokromatozom ne bi se trebala podvrgavati genetskom testiranju dok se drugi roditelj ne testira. Ako je drugi roditelj normalan (tj. nema defekata gena C282Y, S65C ili H63D), sva će djeca biti jednostavni heterozigoti i neće imati povećan rizik od preopterećenja željezom. Probir na hepatocelularni karcinom rezerviran je za osobe s nasljednom hemokromatozom i cirozom.
Hepatocelularni karcinom odgovoran je za približno 30 % smrti u bolesnika s nasljednom hemokromatozom. Hepatocelularni karcinom vrlo se rijetko pojavljuje u bolesnika bez ciroze, što naglašava važnost ranog otkrivanja i liječenja preopterećenja željezom. Bolesnici s nasljednom hemokromatozom i cirozom trebaju ići na ultrazvučni probir svakih šest do 12 mjeseci. Ako se na jetri pronađe lezija manja od 1 cm, interval probira se mijenja na svaka tri do šest mjeseci. Ako je lezija 1 cm ili veća, preporuča se MSCT i biopsija jetre. Rana flebotomija potiče regresiju ciroze i smanjuje morbiditet i mortalitet
ZAKLJUČAK
Hemokromatoza je čest poremećaj koji podrazumijeva varijabilne kliničke manifestacije koji se razlikuju ovisno o spolu. Poremećaj je povezan sa povećanom smrtnosti u muškaraca. Pravovremena klinička konstatacija kroz obiteljski screening i evaluaciju pojedinaca sa sugestivnim biokemijskim ili kliničkim obilježjima otkrit će bolest u najranijoj fazi. Sve osobe sa hemokromatozom i povišenim serumskim razinama feritina trebaju biti podvrgnute liječenju. Glavne kliničke manifestacije bolesti su bolest jetre i artritis. Osobe sa uznapredovalom jetrenom fibrozom trebaju se liječiti i biti dugoročno praćene radi pravovremenog otkrivanja primarnog karcinoma jetre. Taj se rizik bitno smanjuje u pacijenata sa cirozom u kojih fibroza terapijom regredira do stadija F2 ili nižeg. Svi odrasli sa hemokromatozom trebaju biti upozoreni na rizik nastanka kolorektalnog karcinoma i karcinoma dojke i treba im dati savjet za adekvatan screening.
Algoritam za dijagnozu nasljedne hemokromatoze u odraslih od 18 godina i starijih.
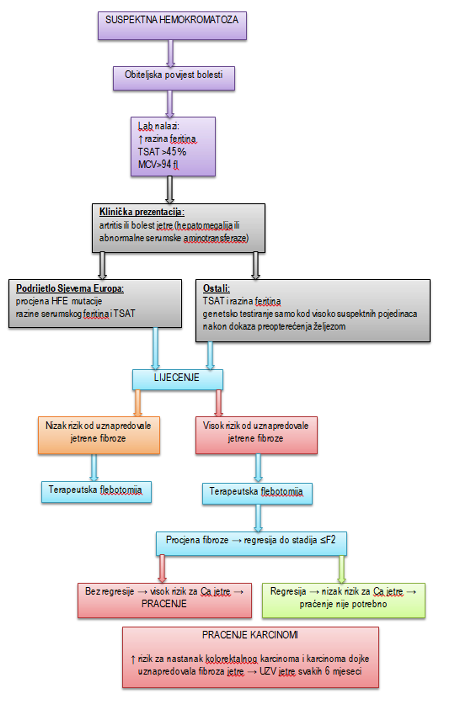
4.OBLIKOVANJE ALTERNATIVNIH PUTEVA DJELOVANJA I IMPLEMENTACIJE PROMJENE
Zadaća obiteljskog liječnika je posumnjati na bolest u osoba koje se prezentiraju nespecifičnim simptomima poput umora, letargije i artralgija (najčešće), a kod kojih u osnovnim laboratorijskim nalazima imamo povišene vrijednosti jetrenih transaminaza. Tada je potrebno provesti daljnju laboratorijsku analizu u smislu određivanja feritina i TSAT, te ukoliko nađemo povišene vrijednosti pacijenta upućujemo na daljnju obradu gastroenterologu koji dalje preuzima obradu i liječenje. Važno je pacijentu savjetovati obaveznu restrikciju alkohola. Ukoliko se UZV pregledom abdomena nađe uznapredovala fibroza ili ciroza jetre pacijente je također potrebno upozoriti na povećani rizik od nastanka kolorektalnog karcinoma i karcinoma dojke te ih u skladu s time uputiti na preventivne preglede. Nadalje, ukoliko pacijent boluje od neke kronične bolesti istu nastavljamo redovito kontrolirati uz izbjegavanje korištenja hepatotoksičnih lijekova. Najznačajniji su antimikrobni, zatim lijekovi s učinkom na neurološki sustav, statini te analgetici.
Najčešći hepatotoksični lijekovi u PZZ
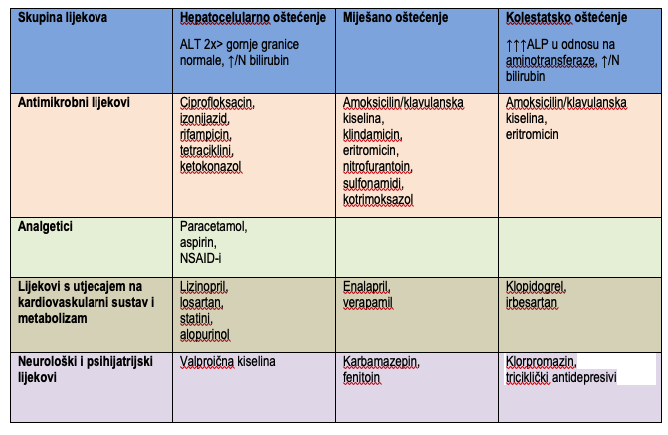
Literatura:
John K. Olynyk, M.D. and Grant A. Ramm, Ph.D. ,Hemochromatosis, The New England Journal of Medicine 2022;387:2159-70
Nemeth E, Tuttle MS, Powelson J, et al:Nemeth E, Tuttle MS, Powelson J, et al: Hepcidin regulates cellular iron efflux by binding to ferroportin and inducing its internalization. Science 306(5704):2090-2093, 2004.
https://www.aafp.org/pubs/afp/issues/2013/0201/p183.html
